İlaçlarla kullanılmaya uygun malzemelerden üretilmiş bir etiket seçmek, ilaç ürünlerinin güvenliğinin sağlanması açısından kritik öneme sahiptir. UPM Raflatac olarak, titizlikle önceden test edilen, kullanım amacına uygun olarak geçerli düzenleme gerekliliklerini karşılayan ve uzun süreli tedarik güvencesi sunan malzemeler kullanarak etiketlerimizin güvenliğini sağlıyoruz.
Düzenlemelerle tamamen uyumlu ilaç etiketleri
Düzenlemelerle uyumluluğa sahip olacak şekilde geliştirilen, formüle edilen ve üretilen ilaç etiketleri
İnsanları koruma
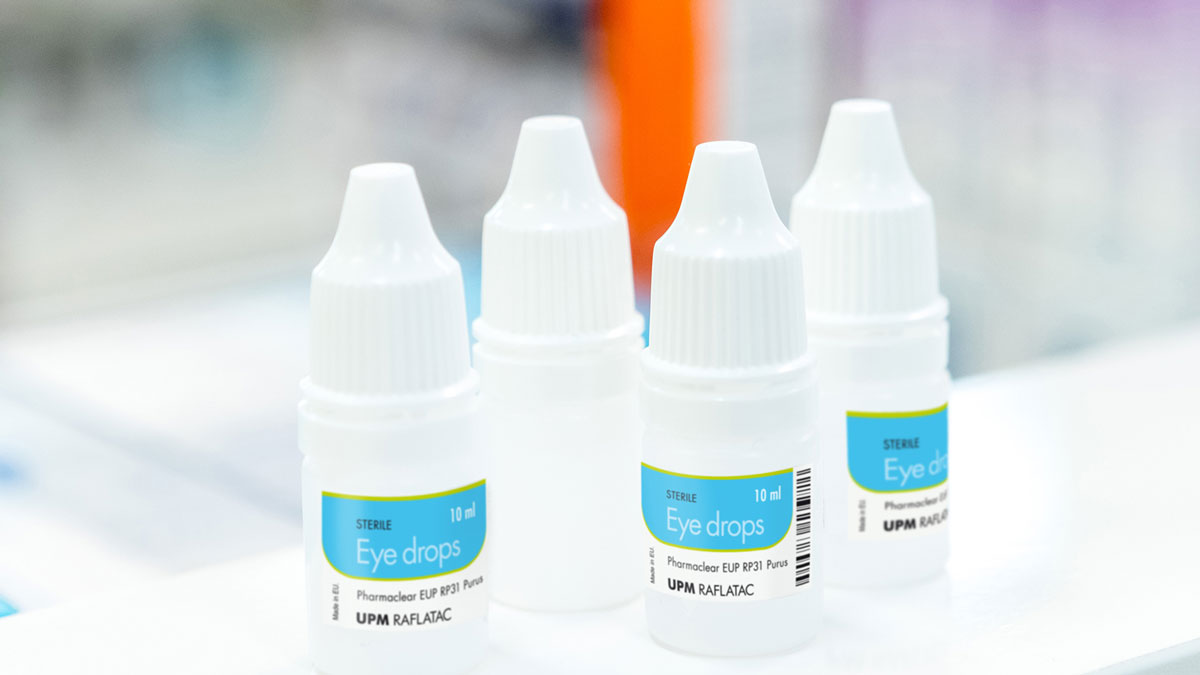
Düşük migrasyon özellikli ilaç etiketleri
Etiketler çok önemli tıbbi bilgiler barındırarak güvenliğin korunmasında rol oynar. Düşük migrasyon özellikli malzemeler kullanılmasını gerektiren bazı ilaç ürünleri söz konusu olduğunda etiketler endişelere de neden olabilir. Düşük sızma özelliğine sahip etiket gerektirebilecek ilaç ürünlerine göz damlaları, burun spreyleri veya enjeksiyon ürünleri gibi plastik ambalaj içinde paketlenmiş sıvı ilaçlar örnek verilebilir. Seçilen ilaç malzemelerimiz ve gelişmiş yapışkan teknolojimiz, aşağıdakiler gibi sektör yönetmeliklerine uygun olarak geliştirilmiştir:
- Plastik İç Ambalaj Malzemelerine İlişkin EMA (Avrupa İlaç Ajansı)/CVMP/205/04 Yönetmeliği (2005)
- İnsan İlaçlarının ve Biyolojik Ürünlerinin Ambalajlanmasında Kullanılan Konteyner Kapatma Sistemlerine İlişkin FDA (ABD Gıda ve İlaç Dairesi) Kılavuzu (1999)
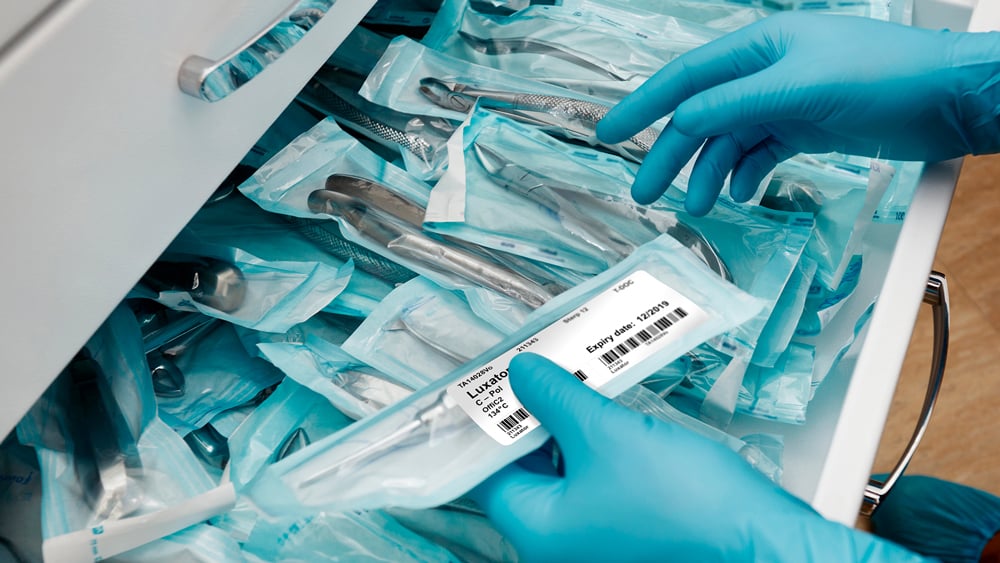
Tıbbi cihaz düzenlemeleri
Tıbbi cihaz düzenlemeleri, baskı ve etiketleme sistemlerinin steril bariyer sistemi işleme, cihaz ve malzemeleriyle uyumlu olmasını ve etiketlerin kullanım noktasına kadar bozulmadan ve okunaklı halde kalmasını gerektirir. Tıbbi cihaz etiketleri, hastaların veya son kullanıcıların cihazın kendisini ve cihazı nasıl kullanıp bakım yapabileceklerini anlamasına yardımcı olur. Tıbbi cihaz düzenlemeleri şunları içerir:
- Yeni oluşturulan küresel Tıbbi Cihaz düzenlemesi, sağlık ürünü tedarik zincirinde tıbbi cihazları işaretlemek ve tanımlamak için bir Benzersiz Cihaz Kimliği (UDI) serileştirme sisteminin benimsenmesini içermektedir. En son UDI düzenleme güncellemelerinden biri, ABD FDA tarafından 2013'te kabul edilene benzer bir sistem olan ve en geç Mayıs 2020'ye kadar yürürlüğe girmesi gereken yeni AB Tıbbi Cihaz Düzenlemesidir [MDR].
- İn Vitro Diyagnostik Düzenlemeleri (IVDR), Avrupa pazarında in vitro diyagnostik tıbbi cihazlarını piyasaya sürmenin, satışa sunmanın ve kullanıma sokmanın yasal dayanağıdır. AB'de İn Vitro Diyagnostik Düzenlemelerinin (IVDR) uygulanması için son tarih Mayıs 2022'dir.
Sahte İlaç Direktifi (2011/62/EU)
Sahte İlaç Direktifi (2011/62/EU) reçeteli ilaçların ve yüksek riskli reçetesiz ilaçların ambalajlanmasını konu alır. Bu direktifle uyumluluk, tüm dünyada ilaç ürünlerinin ambalajlarında izinsiz değiştirme doğrulama özelliklerinin kullanılmasını ve bunların birbiriyle uyumlu hale getirilmesini destekleyen ISO 21976 "Ambalajlama - İlaç ürünü ambalajları için izinsiz değiştirme doğrulama özellikleri" standardında tanımlanmış kanıt bırakan özellikler kullanılarak sağlanır.
Ambalajlama düzenlemeleri
İlaç ve sağlık ürünlerine yönelik etiket malzemelerimiz ambalajlama düzenlemelerine uygun olacak şekilde tasarlanır. Etiket malzemelerimiz, kullanım amaçlarına yönelik olarak ambalajlama ve gıda teması için geçerli tüm düzenleyici ve güvenlik gerekliliklerine uygundur:
- 94/62/EC sayılı AB Direktifi ve daha önce Kuzey Doğu Valileri Birliği (CONEG, ABD) olarak bilinen Toxics in Packaging Clearinghouse (TPCH) ile ilgili ağır metallere ilişkin ambalajlama düzenlemeleri.
- Yapışkanlar, gıda temasına ilişkin Avrupa düzenlemeleri açısından değerlendirilmiştir;
- Gıdalarla temas etmesi amaçlanan malzemeler ve maddeler hakkında 1935/2004 sayılı Gıda Çerçevesi Düzenlemesi (EC) ve
- Gıdalarla temas etmesi amaçlanan malzemelere ve maddelere ilişkin iyi üretim uygulaması hakkında 2023/2006 sayılı Düzenleme (EC).
- FDA Gıdalarla Temas Uyumluluğu:
- FDA 21 CFR §110 - İyi Üretim Uygulamaları (GMP)
Neden özel ilaç etiketleme çözümlerini kullanmalısınız?
Etiketler ürünün yaşam döngüsü boyunca çok önemli tıbbi bilgileri barındırmanın yanı sıra ürün içeriğinin korunmasında ve mühürlenmesinde de rol oynar. Yüksek düzeyde dayanıklılık, yüksek baskı kalitesi, yüksek performans, düzenlemelere uygunluk ve ürün güvenliğini korumak bir etiketin sahip olması gereken özelliklerden sadece birkaçıdır. Marka ve işletmeler, özel ilaç etiketi çözümlerini tercih ederek etiket malzemelerinin şu özelliklere sahip olduğundan emin olabilir:
- İlaç uygulamaları için tasarlanmış ve önceden test edilmiş
- Ürün güvenliği ve yasal uyumluluk göz önünde bulundurularak geliştirilmiş
- Değişiklik yönetimi bildirimleri ve güvence altına alınmış bulunurlukla uzun süreli bulunurluğu ve istikrarlı bir şekilde tedarik edilmesi garanti edilmiş
- Son kullanıcı ürün düzenleme doğrulamasına yardımcı olmak amacıyla bir belgelendirme hizmetiyle desteklenmiş